14.A【解析】根据装置图,高锰酸钾亐浓盐酸反应的化学反应方程式为:2KMnO4+16HCl(浓)2KCl+5C12↑+2MnCl28H2O,根据方程式中元素化合价的变化可以得出氧化剂和还原剂物质的量之比为1:5,故A错误;制备的氯气中含有少量挥发出来的氯化氢气体,可用饱和食盐水除去,装置B具有除杂和平衡压强的作用,故B正确;氯气氧化溴化钠生成溴,故C正确;装置A制备岀来的氯气,与装置C中的溴化钠反应生成溴单质,将生成的液溴滴加到D装置,可生成碘单质,证明氯、溴、碘的非金属性逐渐减弱,但实验过程中要注意及时关闭B、D装置之间的活塞,防止过量的氯气与碘化钾反应,故D正确。选A。
发布时间:2020-10-28 22:43:45
题目来源:百师联盟2021届高三开学摸底联考(新高考卷)化学试题
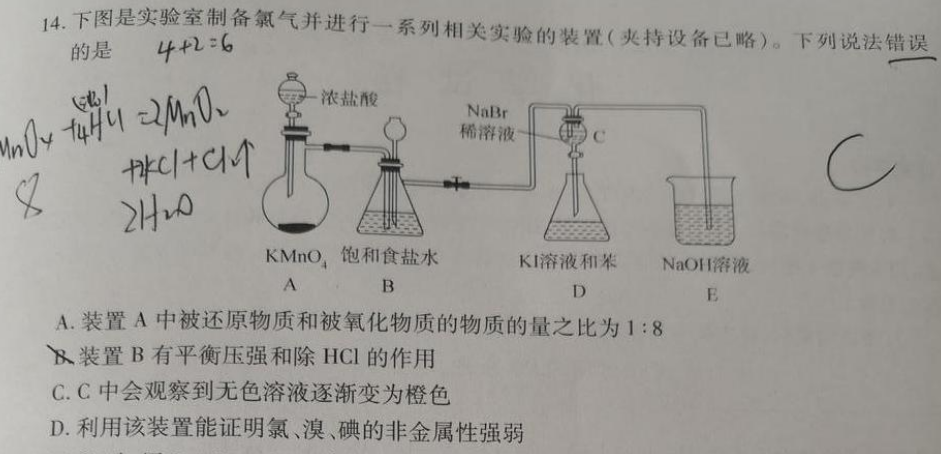
14.下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。下列说法错误的是4+2=6n0+40浓盐酸 NaBr稀溶液cC1+C1个2H0KMnO饱和食盐水K溶液和苯NaOH溶液ABDEA.装置A中被还原物质和被氧化物质的物质的量之比为1:8装置B有平衡压强和除HCl的作用C.C中会观察到无色溶液逐渐变为橙色D.利用该装置能证明氯、溴、碘的非金属性强弱
答案解析
点击查看解析
Copyright ©2016-2023 All Rights Reserved. 答案解析网版权所有 鲁ICP备18002841号-2 增值电信许可鲁B2-20210786
答案解析网 版权所有 鲁公网安备 37150202000430号 教APP备3700145号

扫码下载
答案解析网APP